Lithiumfluorphosphate sowie deren Verwendung als Leitsalze
The invention concerns novel lithium fluorophosphates of general formula Li<+>[PFa(CHbFc(CF3)d)e]<-> (I) in which: a designates 1, 2, 3, 4 or 5; b designates 0 or 1, c designates 0, 1, 2 or 3; d designates 0, 1, 2 or 3; and e designates 1, 2, 3 or 4, provided that the total of a + e equals 6, the total of b + c + d equals 3, and b and c do not simultaneously designate 0, and provided that the ligands (CHbFc(CF3)d) can be different. The invention further concerns a process for preparing these compounds, their use in electrolytes, and lithium batteries produced with these electrolytes.
Die Erfindung betrifft neue Lithiumfluorphosphaten der allgemeinen Formel
Li[PFa(CHbFc(CF)d)e], (I)
worina 1, 2, 3, 4 oder 5,b 0 oder 1c 0, 1, 2 oder 3,d 0, 1, 2 oder 3 unde 1, 2, 3 oder 4bedeuten, mit der Bedingung, daß die Summe a + e gleich 6, die Summe b + c + d gleich 3 ist und b und c nicht gleichzeitig 0 bedeuten, unter der Voraussetzung daß die Liganden (CHbFc(CF)d) unterschiedlich sein können,ein Verfahren zur Herstellung dieser Verbindungen, deren Verwendung in Elektrolyten,sowie mit diesen Elektrolyten hergestellte Lithiumbatterien.
Die Erfindung betrifft ebenfalls Verbindungen der allgemeinen Formel
[PFa(CHbFc(CF)d)e] (Ia),
worin, wie in Formel (I)b 0 oder 1c 0, 1, 2 oder 3,d 0, 1, 2 oder 3 unde 1, 2, 3 oder 4,jedocha 1, 2, 3 oder 4bedeuten,die als Zwischenprodukte zur Herstellung von Verbindungen der Formel (I) benötigt werden.
Üblicherweise wird in Lithium-Sekundärbatterien Lithiumhexafluorphosphat als Leitsalz verwendet. Nachteilig ist, daß dieses Salz relativ wenig hydrolysestabil ist. Es wurden daher verschiedenste Versuche unternommen einen Ersatz für dieses Salz zu finden. Beispielsweise werden in WO 88/03331 Salze cyclischer Perfluoralkanbis(sulfonyl)imide, u. a. auch deren Lithium-Salze, beschrieben, die als Leitsalze in nichtwäßrigen Elektrolyten für Lithium-Sekundärbatterien eingesetzt werden können. Wie Versuche ergeben haben, lassen sich solche Verbindungen jedoch nur unter großem Aufwand herstellen und müssen nach der Synthese von unerwünschten Nebenprodukten befreit werden. Die Aufreinigung der Salze ist unerläßlich, da für die Anwendung als Bestandteil von Batterieelektrolyten reproduzierbare Eigenschaften unerläßlich sind.
Aufgabe der Erfindung ist es daher, geeignete Leitsalze für Elektrolyte zur Verwendung in Lithiumbatterien zur Verfügung zu stellen. Aufgabe der Erfindung ist es auch ein Verfahren zur Verfügung zu steilen, wodurch in einfacher und preiswerter Weise die erfindungsgemäßen Leitsalze hergestellt werden können.
Die erfindungsgemäße Aufgabe wird gelöst durch neue Lithiumfluorphosphate der allgemeinen Formel
Li[PFa(CHbFc(CF)d)e], (I)
worina 1, 2, 3, 4 oder 5,b 0 oder 1c 0, 1, 2 oder 3,d 0, 1, 2 oder 3 unde 1, 2, 3 oder 4bedeuten, mit der Bedingung, daß die Summe a + e gleich 6, die Summe b + c + d gleich 3 ist und b und c nicht gleichzeitig 0 bedeuten, und mit der Bedingung, daß die Liganden (CHbFc(CF)d) unterschiedlich sein können,die das in Lithium-Sekundärbatterien üblicherweise als Leitsalz
verwendete Lithiumhexafluorphosphat ersetzen können, aber auch im Gemisch mit diesen eingesetzt werden können.
Gegenstand der Erfindung sind daher sowohl die neuen erfindungsgemäßen Salze der Formel (I) als auch ein Verfahren zu ihrer Herstellung und Verbindungen der allgemeinen Formel (Ia),
[PFa(CHbFc(CF)d)e] (Ia),
worin, wie in Formel (I)b 0 oder 1c 0, 1, 2 oder 3,d 0, 1, 2 oder 3 unde 1, 2, 3 oder 4,jedocha 1, 2, 3 oder 4bedeuten,die als Zwischenprodukte zur Herstellung der Salze gemäß der allgemeinen Formel (I) benötigt werden.
Gegenstand der Erfindung sind schließlich auch Elektrolyte, die die erfindungsgemäßen Salze enthalten und elektrochemische Zellen, hergestellt unter Verwendung dieser Elektrolyte. Solche elektrochemischen Zellen können sowohl primäre als auch sekundäre Batterien sein, die die Lithiumverbindungen gemäß Formel (I) enthalten.
Insbesondere sind die folgenden Lithiumsalze
deren Verwendung als Leitsalze in Elektrolyten, Elektrolyte, die diese enthalten, sowie Lithiumbatterien, in denen diese Verbindungen als Leitsalze enthalten sind, Gegenstand der Erfindung.
Zur Herstellung der erfindungsgemäßen Salze werden in einer ersten Stufe geeignete Di-chlor-mono-, Chlor-di-alkylphosphine, Di-Fluor-mono-, Fluor-dialkylphosphine; Chlordifluor-, Dichlorfluor-, Trifluor-dialkyl-phosphorane oder Tetrachlorfluor-alkylphosphorane, Chlor- oder Fluor-anhydrid-alkylphosphinsäure oder Dichlor- oder Difluor-anhydrid-alkylphosphonsäure, Chlor- oder Fluor-dialkylphosphinoxide oder Trialkyphophinoxide in einem Lösungsmittel aufgenommen und in bekannter Weise elektrochemisch bei einer Temperatur von -15 bis 20ºC unter Normaldruck fluoriert. Als Lösungsmittel für diese Reaktion ist Fluorwasserstoffsäure geeignet. Die Fluorierungsreaktion wird abgebrochen, wenn 90 bis 150%, insbesondere 110 bis 130%, der theoretischen Elektrizitätsmenge aufgenommen worden sind. Dieses wird festgestellt durch coulombmetrische Messung.
Je nach Dauer der Reaktion werden Produktgemische erhalten, in denen sowohl mit Fluor völlig abgesättigte Verbindungen enthalten sind als auch solche, die partiell fluoriert sind. Beispielsweise werden bei der Fluorierung von Chlor-diisopropylphosphin die folgenden Produkte erhalten:
Die eigentlichen erfindungsgemäßen Salze der Formel (I) werden erhalten, indem die in der ersten Stufe erhaltenen fluorierten Alkylphosphorane als Produktgemisch, vorzugsweise nach destillativer Auftrennung unter wasserfreien Bedingungen, in einem geeigneten aprotischen, polaren Lösungsmittel, wie z. B. Dimethylether, Dimethoxyethane oder deren Gemische, aufgenommen werden und mit Lithiumfluorid, je nach Reaktivität, bei einer Temperatur von 0 bis 60ºC, vorzugsweise unter Beibehaltung
von Raumtemperatur, zu Verbindungen der Formel (I) umgesetzt werden.
In den erfindungsgemäßen Elektrolyten sind sowohl die reinen Verbindungen der Formel (I) als auch die durch die Fluorierungsreaktion erhaltenen Gemische einsetzbar. Vorzugsweise aufgrund der Reproduzierbarkeit der Elektrolyteigenschaften werden die reinen Verbindungen zur Herstellung der Elektrolytlösungen eingesetzt.
Überraschenderweise wurde durch Versuche gefunden, daß Verbindungen der Formel (I) in aprotischen polaren Lösungsmitteln bei Raumtemperatur hydrolysestabil sind, und zwar insbesondere jene, deren Alkylreste völlig durch Fluor abgesättigt sind. Dabei nimmt die Hydrolysestabilität mit der Zahl der Fluoratome im Molekül zu.
Unter aprotischen, polaren Lösungsmitteln sind solche wie
- Nitrile Acetonitril oder Benzonitril,
- Ether Diethylether, Dimethoxyethan, Tetrahydrofuran, Dioxan oder Dimethyltetrahydrofuran,
- Ester Methyl- oder Ethylester der Ameisensäure, der Essigsäure, der Propionsäure, aber auch cyclische Ester, wie Butyrolacton, und organische Carbonate, wie z. B. Dimethylcarbonat, Diethylcarbonat, Ethyl-methylcarbonat, Ethylencarbonat, oder Propylencarbonat,
- Amide Dimethylformamid, Diethylformamid, N-Methylpyrolidin
oder
- Sulfone Dimethylsulfon, Tetramethylensulfon oder andere Sulfolane
zu verstehen.
Die erfindungsgemäßen Salze weisen außerdem in diesen Lösungsmitteln eine hervorragende Löslichkeit auf, und insbesondere die durch Fluor völlig abgesättigten Verbindungen sind wenig hygroskopisch.
Versuche haben gezeigt, daß diese Verbindungen außerordentlich stabil sind. Bei trockener Lagerung im festen Zustand weisen perfluorierte Verbindungen bei Temperatur unterhalb von 100ºC keine Zersetzung auf. Auch bei weiterer Temperaturerhöhung erweisen sie sich als thermisch stabil. Erst bei Temperaturen oberhalb von 130ºC zeigen sich leichte Verfärbungen.
Auch bei Lagerung in Lösung, z. B. in Dimethoxyethan, sind selbst nach Wochen keine Farbveränderungen feststellbar oder Zersetzungsprodukte nachzuweisen.
Aus diesem Grund eignen sich die erfindungsgemäßen Verbindungen, insbesondere die Verbindungen der Formeln III, IV, V, VI und VII, bereits vorzüglich als Leitsalze in nichtwäßrigen Elektrolyten für Lithiumbatterien.
Weiterhin weisen Elektrolytlösungen, die diese Verbindungen enthalten, bemerkenswerte chemische und elektrochemische Stabilitäten auf. Insbesondere kann eine Oxidation des korrespondierenden Anions vor der Lithiumabscheidung nicht nachgewiesen werden.
Derartige Elektrolyte enthalten neben Lithium-organischen Salzen, wie es die erfindungsgemäßen Verbindungen der Formel (I) sind, ein oder mehrere nichtwäßrige, organische Lösungsmittel und gegebenenfalls weitere Zusatzstoffe. Nach Wunsch können neben den erfindungsgemäßen Verbindungen auch bereits bekannte Lithiumsalze als Leitsalze dem Elektrolyten zugesetzt sein. Nähere Einzelheiten zu derartigen Elektrolyten und dem Aufbau und der Funktionsweise von Lithiumbatterien sind dem Fachmann auf diesem Technologiegebiet bekannt. Die erfindungsgemäßen Verbindungen können in völliger Analogie zu für diese Anwendung bekannten Lithiumverbindungen eingesetzt werden und zeigen hierbei außergewöhnlich hohe Stabilitäten. Entsprechende Batteriezellen zeigen vorzügliche Eigenschaften bezüglich Kapazität und Spannungskonstanz, sowie eine uneingeschränkte Funktionsfähigkeit
über eine überdurchschnittlich hohe Zahl an Lade-Entlade-Zyklen hinweg.
Die im folgenden gegebenen Beispiele werden zur besseren Veranschaulichung der vorliegenden Erfindung gegeben, sind jedoch nicht dazu geeignet, die Erfindung auf die hierin offenbarten Merkmale zu beschränken.
BeispieleBeispiel 1Bis-(heptafluor-i-propyl)-trifluorphosphoran (IIa) sowie dessen Derivate
Nach dem Simons-Prozeß wird Di-i-Propylchlorphosphin elektrochemisch in einer elektrochemischen Zelle, die Fluorwasserstoffsäure als Lösungsmittel enthält, fluoriert. Die verwendete zylindrische Zelle mit einem Volumen von 310 cm³, ausgestattet mit Nickel-Anoden einer effektiven Fläche von S 3,75 dm², und Kathoden der gleichen effektiven Fläche. Weiterhin ist die Zelle mit einem Kühlkondensator ausgestattet. Die Zelltemperatur wird während der Elektrolyse bei -5ºC gehalten und die des Kondensators bei -30ºC.
57 g Di-i-Propylchlorphosphin, gelöst in 200 g Fluorwasserstoffsäure, werden portionsweise zu 235 g zuvor elektrolysierter Fluorwasserstoffsäure gegeben, und zwar in folgender Weise:
Gasförmige Produkte, die den Kühlkondensator und zwei PTFE-Fallen passiert haben, werden auf -78ºC gekühlt.
Die Elektrolyse, die bei einer Spannung von 4,4-5,4 V und einer Flußdichte von 0,30-0,53 Ndm² durchgeführt wird, ist beendet nach einem Stromverbrauch von 420 A h (131% der Theorie), wobei etwa
220 g flüssiges Produkt aus der Zelle aufgefangen werden. Nachdem die Temperatur auf -20ºC eingestellt worden ist und die untere Phase von der Fluorwasserstoff-Phase abgetrennt worden ist, werden 18 g Rohprodukt erhalten. NMR ¹F-spektroskopisch lassen sich darin 75% Bis-(heptafluorisopropyl)-trifluorphosphoran, (IIa), 15% Heptafluor-i-propyl-(1,1,1,3,3,3-hexafluor-i-propyl)-trifluorphospho-ran (IIb) und Bis-(hexa-1,1,1,3,3,3-hexafluor-i-propyl)-trifluorphosphoran (IIc) nachweisen.
Durch fraktionierte Destillation kann dieses Gemisch aufgetrennt werden in Fraktionen, die jeweils eine dieser Verbindungen als Hauptkomponente enthält. Außerdem werden nach der Abtrennung von der Fluorwasserstoff-Phase 33 g bei niedrigen Temperaturen flüssige Produkte aus den Kühlfallen erhalten. NMR ¹F-spektroskopische Untersuchungen zeigen, daß es sich hierbei vorwiegend um Heptafluor-i-propyl-tetrafluorphosphoran (IId), 1,1,1,3,3,3-hexafluor-i-propyl-tetrafluorphosphoran (IIe) und Perfluorpropan handelt. Durch Erhitzen auf 20ºC läßt sich das Perfluorpropan abdestillieren. Der Rückstand läßt sich durch fraktionierte Destillation auftrennen in Fraktionen, die Heptafluor-i-propyl-tetrafluorphosphoran(IId) oder 1,1,1,3,3,3-Hexafluorisopropyltetrafluorphosphorane (IIe) als Hauptkomponenten enthalten.
Die erhaltenen Verbindungen lassen sich durch folgende Daten charakterisieren:
Bis-(heptafluorisopropyl)-trifluorphosphoran (IIa):
NMR ¹F, ppm: -39,72 dtm (3 F¹)-70,15 m (12 F³)-171,78 dm (2 F²)J²F1F2 = 8,0 HzNMR ³P, ppm: -26,0 qtmJ¹P,F rg61 rt5 1 rg rt sg9 = 1083 HzJ²P,F rg61 rt5 2 rg rt sg9 = 102 HzJ³P,F rg61 rt5 3 rg rt sg9 = 4,9 Hz
Heptafluor-i-propyl-(1,1,1,3,3,3-hexafluor-i-propyl)-trifluorphospho-ran (IIb):
NMR ¹F, ppm: -33,10 dm (3 F¹)-59,56 m (6 F)-70,26 m(6F³)-171,90 m (1F²)NMR ³P, ppm: -23,2 qdmJ¹P,F rg61 rt5 1 rg rt sg9 = 1014,0 HzJ²P,F rg61 rt5 2 rg rt sg9 = 99,0 HzJ³P,F rg61 rt5 3 rg rt sg9 = 5,2 HzJ³P,F rg61 rt5 4 rg rt sg9 = 5,7 HzJ²P,H = 11,0 HzNMR 'H, ppm: 3,9 dm
Bis-(hexa-1,1,1,3,3,3-hexafluor-i-propyl)-trifluorphosphoran (IIc):
NMR ¹F, ppm: -25,96 dm (3 F¹)-59,51 m (12 F²)NMR ³P, ppm: -20,69 qmJ¹P,F rg61 rt5 1 rg rt sg9 = 9600 HzJ³P,F rg61 rt5 2 rg rt sg9 = 11,3 HzNMR 'H, ppm: 3,9 dm
Heptafluor-i-propyl-tetrafluorphosphoran (IId):
NMR ¹F, ppm (CDCN-film; -30ºC):-50,10 dm (4 F¹)-72,22 m (6 F³)-172,83 dm (1F²)NMR ³P, ppm (CDCOCD-film; -40ºC):-55,3 pdsepJ¹P,F rg61 rt5 1 rg rt sg9 = 1042,0 HzJ²P,F rg61 rt5 2 rg rt sg9 = 100,0 HzJ³P,F rg61 rt5 3 rg rt sg9 = 6,0 Hz
1,1,1,3,3,3-Hexafluor-i-propyl-tetrafluorphosphorane (IIe):
NMR ¹F, ppm (CDCN-film; -30ºC):-40,90 dm (4 F¹)-61,8 m (6 F²)NMR ³P, ppm (CDCOCD-film; -40ºC):-50,8 pdsepJ¹P,F rg61 rt5 1 rg rt sg9 = 1003,0 HzJ³P,F rg61 rt5 2 rg rt sg9 = 14,0 HzJ²P,H = 27,0 HzBeispiel 2Tris-(pentafluorethvl)-difluorphosphoran (Va)
Analog zu der Durchführung beschrieben in Beispiel 1 werden aus 69 g Triethylphosphinoxid 70 g Tris-(pentafluorethyl)-difluorphosphoran (Va) hergestellt. NMR ³P-spektroskopische Daten entsprechen denen in der Literatur (V.J. Semenii et. Al.; Zh. Obshch. Khim. (Russ.) 1985 Vol. 55, 12, 2716-2720):
NMR ³P, (CDCOCD-film; 85%-ige HPO als innerer Standard), ppm:-47,55 tsepJ¹P,F = 1003,0 HzJ²P,F = 122,0 HzBeispiel 3Lithium Bis-(heptafluor-i-propyl)-tetrafluornhosphonat (III)
Zu einer in einem aus PTFE bestehenden Reaktionsgefäß vorgelegten Lösung, bestehend aus 0,82 g (0,031 mol) LiF und 60 ml vorgetrocknetem Dimethoxyethan, werden unter Feuchtigkeitsausschluß langsam 12 g (0,028 mol) Bis-(heptafluor-i-propyl)-trifluorphosphoran(IIa) unter Rühren mit einem Magnetrührer hinzugegeben, wobei die Temperatur durch Kühlung in einen Eiswasserbad auf Raumtemperatur gehalten wird. Anschließend wird bei gleicher Temperatur für eine Stunde nachgerührt und noch geringe Mengen metallischen Lithiums hinzugefügt. Die Reaktionsmischung wird für 24 bei Raumtemperatur gehalten, anschließend filtriert und kann direkt als Elektrolyt für wiederaufladbare Batterien verwendet werden. Das während der Reaktion gebildete Lithium-bis-(heptafluor-i-propyl)-tetrafluorphosphat (III) kann jedoch auch isoliert werden, indem das Lösungsmittel unter Hochvakuum abdestilliert wird.
Isoliert wird ein Lithium-Komplexsalz (III), Li[(i-CH)PF] 2 DME,Smp.: 126-128ºC; thermisch stabil bis 130ºC.Analyse: Litheoretisch: 0,93%gefunden: 1,15%.
Das Kristallwasser kann entfernt werden, indem das Komplexsalz (III) für mehrere Tage im Hochvakuum auf eine Temperatur von 80ºC erwärmt wird.
Beispiel 3a
Zur Herstellung von erfindungsgemäßen Lithiumsalzen kann die in Beispiel 1 erhaltene Fluorphosphanmischung direkt ohne vorherige fraktionierte Destillation verwendet werden.
16 g einer Fluorphosphanmischung aus Beispiel 1, die 75% der Verbindung (IIa), 15% der Verbindung (IIb) und 10% der Verbindung (IIc) enthält, wurde, wie oben beschrieben, zu einer Lösung bestehend aus 1,0 g LiF und 80 ml trockenem DME, gegeben. Auch diese Lösung kann nach dem Filtrieren direkt als Elektrolyt eingesetzt werden. Die Li-Salze können aber auch aus der Lösung auskristallisiert werden, indem vorgetrocknetes Hexan zu der DME-Lösung gegeben wird. Durch Umkristallisieren des erhaltenen Produkts mit einem Lösungsmittelgemisch bestehend aus getrocknetem DME und Dibutylether (1 : 2) werden 13,6 g Lithium Bis-(heptafluor-i-propyl)-tetrafluorphosphonat (III) zusammen mit 6% Lithium-heptafluorisopropyl(1,1,1,3,3,3-hexafluor-i-propyl)-tetraflu-orphosphonat (IV) erhalten.
Die Struktur der Salze (III) und (IV) wurde nachgewiesen durch NMR¹F- und ³P-Spektroskopie. NMR-Spektren wurden in CDCOCD-Lösungen mit CClF und im anderen Fall 85%-iger HPO als Standards gemessen.
Lithium Bis-(heptafluor-i-propyl)-tetrafluornhosphonat (III)NMR ¹F, ppm: -58,14 dm (4 F¹)-71,07 pdd (12 F³)-184,40 dpsep (2 F²)J³F rg61 rt5 1 rg rt sg9 ,F rg61 rt5 2 rg rt sg9 = 4,0 HzJF rg61 rt5 1 rg rt sg9 ,F rg61 rt5 3 rg rt sg9 = 10,9 HzJ³F rg61 rt5 2 rg rt sg9 ,F rg61 rt5 3 rg rt sg9 = 4,7 Hz
NMR ³P, ppm: -149,27 ptm- 148,42 ptm (CDCN-Lösung)J¹P,F rg61 rt5 1 rg rt sg9 = 943,0 HzJ²P,F rg61 rt5 2 rg rt sg9 = 75,0 HzJ³P,F rg61 rt5 3 rg rt sg9 = 8,2 HzLithium-heptafluorisopropyl(1,1,1,3,3,3-hexafluor-i-propyl)-tetraflu-orphosphonat (IV)NMR ¹F, ppm: -47,20 dddm (4 F¹)-58,01 dpd (6 F)-70,79 pdd (6 F³)-183,50 dm (1 F²)J³F rg61 rt5 1 rg rt sg9 ,F rg61 rt5 2 rg rt sg9 = 4,1 HzJ³H,F rg61 rt5 1 rg rt sg9 = 4,1 HzJ³F2,F rg61 rt5 3 rg rt sg9 = 8,0 HzJF1,F rg61 rt5 3 rg rt sg9 = 11,5 HzJF1,F rg61 rt5 4 rg rt sg9 = 11,5 HzNMR³P, ppm: -147,37 pdmJ¹P,F rg61 rt5 1 rg rt sg9 = 928,0 HzJ³P,F rg61 rt5 2 rg rt sg9 = 74,5 HzJ³P,F rg61 rt5 3 rg rt sg9 = 8,3 HzJ³P,F rg61 rt5 4 rg rt sg9 = 11,4 HzBeispiel 4Lithium (heptafluor-i-propyl-pentafluorphosphonat) (VIII)
Lithium (heptafluor-i-propyl-pentafluorphosphonat) (VIII) wird in analoger Weise erhalten, wie in Beispiel 3 beschrieben, durch Reaktion von Fluorphosphoran (IId) mit LiF in trockenem Dimethoxyethan. Wie beschrieben, kann die nach dem Filtrieren erhaltene Lösung direkt als Elektrolytlösung eingesetzt werden oder das obengenannte Salz isoliert werden, indem das Lösungsmittel
unter Hochvakuum abdestilliert wird oder durch Auskristallisation, hervorgerufen durch Zugabe von Hexan.
Die Mischung der Fluorphosphorane, erhalten nach Beispiel 1, kann ebenfalls zur Herstellung von Elektrolytlösungen verwendet werden, indem man sie mit LiF ohne vorherige Reinigung umsetzt. Die Lösung der beiden Lithiumsalze (VIII) und (IX), die in diesem Fall erhalten wird, kann ebenso als Elektrolyt für Lithiumbatterien verwendet werden.
Beide Salze können in gleicher Weise, wie oben beschrieben, isoliert werden.
Lithium-heptafluor-i-propyl-pentafluorphosphonat (VIII)NMR ¹F, ppm: (Lösungsmittel: CDCOCD; Standard: CClF)-62,62 dddsep (4 F¹)-73,13 p (1 F²)-71,49 pdd (6 F)-183,72 dpsepm (1 F³)J²F rg61 rt5 1 rg rt sg9 ,F rg61 rt5 2 rg rt sg9 = 45,4 HzJ³F rg61 rt5 1 rg rt sg9 ,F rg61 rt5 3 rg rt sg9 = 3,6 HzJ³F rg61 rt5 3 rg rt sg9 ,F rg61 rt5 4 rg rt sg9 = 4,2 HzJF rg61 rt5 1 rg rt sg9 ,F rg61 rt5 4 rg rt sg9 = 11,4 HzNMR ³P, ppm: (Lösungsmittel: CDCN; Standard: 85% HPO)-148,16 pddsepJ¹P,F rg61 rt5 1 rg rt sg9 = 841,0 HzJ¹P,F rg61 rt5 2 rg rt sg9 = 717,0 HzJ²P,F rg61 rt5 3 rg rt sg9 = 68,7 HzJ³P,F rg61 rt5 4 rg rt sg9 = 4,9 Hz
Lithium-1,1,1,3,3,3-hexafluor-i-propyl-pentafluorphosphonat (IX)NMR ¹F, ppm: (Lösungsmittel: CDCOCD; Standard: CClF)-52,95 dddsep (4 F¹)-69,04 p (1 F²)-59,40 dp (6 F3)J²F rg61 rt5 1 rg rt sg9 ,F rg61 rt5 2 rg rt sg9 = 42,6 HzJ³F rg61 rt5 1 rg rt sg9 ,H = 3,8 HzJF rg61 rt5 1 rg rt sg9 ,F rg61 rt5 3 rg rt sg9 = 12,3 HzNMR ³P, ppm: (Lösungsmittel: CDCN; Standard: 85% HPO)-145,82 pddsepJ¹P,F rg61 rt5 1 rg rt sg9 = 829,0 HzJ¹P,F rg61 rt5 2 rg rt sg9 = 708,0 HzJ²P,H = 29,0 HzJ³P,F rg61 rt5 3 rg rt sg9 = 12,9 Hz
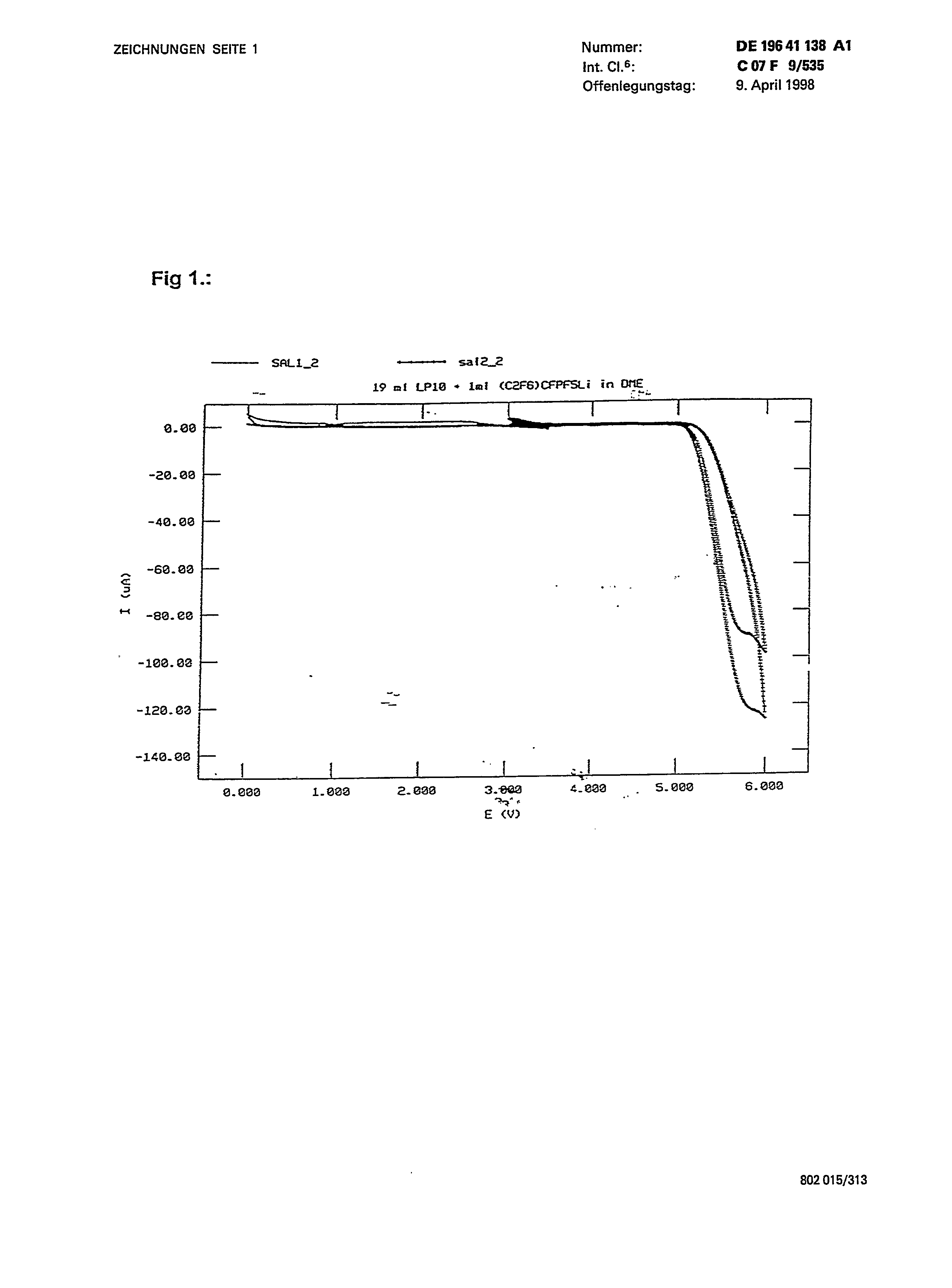
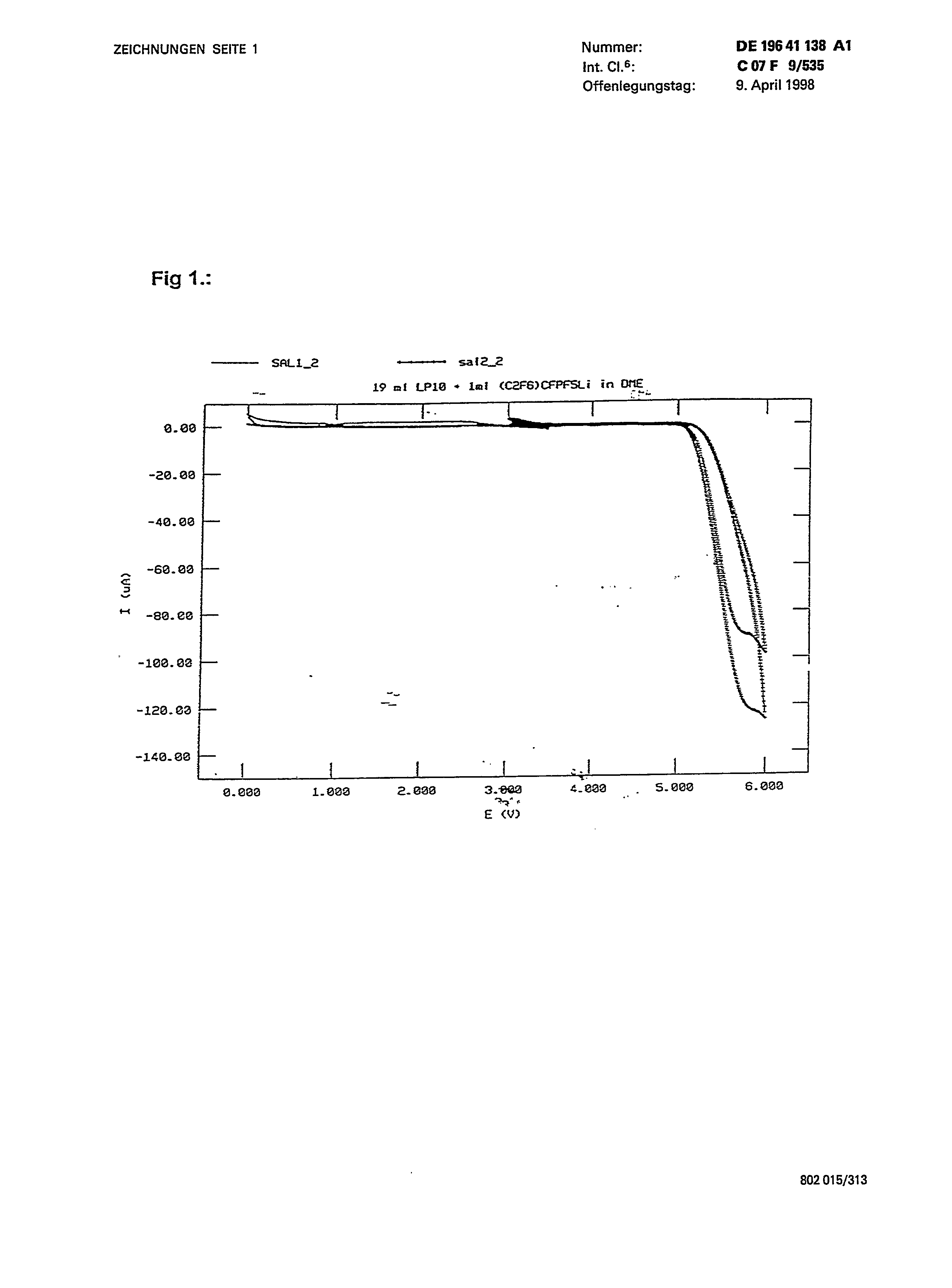
Unter Verwendung von 1 ml Lithium-heptafluor-propyl-pentafluorphosphonat (VIII) gelöst in DME, unter Zusatz von 19 ml LP10, wurden Cyclisierungsversuche durchgeführt. Ergebnisse des ersten und des fünften Cyclisierungsversuchs sind in Fig. 1 dargestellt . . Durchgeführt wurden diese Versuche unter folgenden Bedingungen:Potentialintervall: 0,0-310 V; 3,0-6,0 VÄnderungsrate: 100 mV/sArbeitselektrode: Pt, Oberfläche 1,96E-3 cm2Referenzelektrode: LiMeßelektrode: LiElektrochemische Stabilität: bis zu 5,0 V
Beispiel 5Lithium Tris-(pentafluorethyl)-trifluorphosphonat (V)
Lithium-tris-(pentafluorethyl)-trifluorphosphonat (V) wird ananlog Beispiel 3 erhalten durch Reaktion des entsprechenden analog Beispiel 2 erhaltenen Fluorphosphorans (Va) mit LiF in vorgetrocknetem Dimethoxyethan. Auch in diesem Fall kann die nach der Reaktion und dem Filtrieren erhaltene Reaktionslösung direkt als Elektrolyt verwendet werden oder das Salz (V) durch Abdestillieren des Lösungsmittels unter Hochvakuum oder durch Auskristallisieren, hervorgerufen durch Zugabe von Hexan isoliert werden.Lithium-tris-pentafluorethyl)-trifluorphosphonat (V)NMR ¹F, ppm: (Lösungsmittel: CDCOCD; Standard: CClF)-87,0 d (2 F¹)-43,6 dm (1 F²)-115,3 m (4 F³)-115,7 m (2 F)-79,7 m (3 F)-81,3 m (6 F)NMR ³P, ppm: (Lösungsmittel: CDCN; Standard: 85% HPO)-149,8 tdptJ¹P,F rg61 rt5 1 rg rt sg9 = 902,0 HzJ¹P,F rg61 rt5 2 rg rt sg9 = 889,0 HzJ²P,F rg61 rt5 3 rg rt sg9 = 98,0 HzJ²P,F rg61 rt5 5 rg rt sg9 = 83,0 HzLithium-tris-(pentafluorethyl)-trifIuorphosphonat (V) besitzt einen Smp. von 116-118ºC und ist thermisch stabil bis 130ºC
Fig. 2: Unter Verwendung von 1 ml Lithium-tris-pentafluorethyl)-trifluorphosphonat (V) gelöst in DME, unter Zusatz von 19 ml LP10, wurden Cyclisierungsversuche durchgeführt. Ergebnisse des ersten und des fünften Cyclisierungsversuchs sind in Fig. 2 dargestellt. Durchgeführt wurden diese Versuche unter folgenden Bedingungen:
Potentialintervall: 0,0-3,0 V; 3,0-6,0 VÄnderungsrate: 100 mV/sArbeitselektrode: Pt, Oberfläche 1,96E-3 cm2Referenzelektrode: LiMeßelektrode: LiElektrochemische Stabilität: bis zu 5,0 V
1. Verfahren zur Herstellung von Lithiumfluorphosphaten der allgemeinen Formel
Li[PFa(CHbFc(CF)d)e], (I)
worina 1, 2, 3, 4 oder 5,b 0 oder 1c 0, 1, 2 oder 3,d 0, 1, 2 oder 3 unde 1, 2, 3 oder 4bedeuten, mit der Bedingung, daß die Summe a + e gleich 6, die Summe b + c + d gleich 3 ist und b und c nicht gleichzeitig 0 bedeuten, unter der Voraussetzung daß die Liganden (CHbFc(CF)d) unterschiedlich sein können, dadurch gekennzeichnet, daß
a) Chlor-mono-, Chlor-di, Chlor-tri oder Chlor-tetraalkylphosphine in einem inerten Lösungsmittel elektrochemisch fluoriert werden,
b) das erhaltene Produktgemisch gegebenenfalls destillativ in die verschiedenen Fluorierungsprodukte aufgetrennt wird und
c) die fluorierten Alkylphosphine in einem aprotischen, polaren Lösungsmittel bei einer Temperatur von 0 bis 60ºC mit Lithiumfluorid umgesetzt werden.
2. Verfahren gemäß Anspruch 1, dadurch gekennzeichnet, daß die Fluorierung bei Raumtemperatur und Normaldruck durchgeführt wird.
3. Verfahren gemäß Anspruch 1, dadurch gekennzeichnet, daß die destillative Aufreinigung der Fluorierungsprodukte unter Inertgasatmosphäre erfolgt.
4. Verfahren gemäß Anspruch 1, dadurch gekennzeichnet, daß die Umsetzung mit Lithiumfluorid bei Raumtemperatur erfolgt.
5. Verbindungen der allgemeinen Formel
[PFa(CHbFc(CF)d)e] (Ia),
worin, wie in Formel (I)b 0 oder 1c 0, 1, 2 oder 3,d 0, 1, 2 oder 3 unde 1, 2, 3 oder 4,jedocha 1, 2, 3 oder 4bedeuten,die als Zwischenprodukte zur Herstellung von Verbindungen der Formel (I) gemäß Anspruch 1.
6. Lithiumfluorphosphate der allgemeinen Formel
Li[PFa(CHbFc(CF)d)e], (I)
worina 1, 2, 3, 4 oder 5,b 0 oder 1c 0, 1, 2 oder 3,d 0, 1, 2 oder 3 unde 1, 2, 3 oder 4bedeuten, mit der Bedingung, daß die Summe a + e gleich 6, die Summe b + c + d gleich 3 ist und b und c nicht gleichzeitig 0 bedeuten, unter der Voraussetzung daß die Liganden (CHbFc(CF)d) unterschiedlich sein können.
7. Lithiumfluorphosphate gemäß Anspruch 6
8. Verwendung der Lithiumfluorphosphate gemäß der Ansprüche 6 und 7 als Leitsalze in Lithiumbatterien.
9. Elektrolyte für Lithiumbatterien, enthaltend Lithiumfluorphosphate der allgemeinen Formel (I) gemäß der Ansprüche 6 und 7.
10. Sekundäre Lithiumbatterien enthaltend Elektrolyte gemäß Anspruch 9.